日本原子力研究開発機構 原子力科学研究部門量子ビーム応用研究センター分子構造・機能研究グループの廣本武史研究員は、農研機構花き研究所と共同で、植物の花や果実などの発色を担い、医薬品の原料としても期待される色素アントシアニンを作る酵素の立体構造を、フォトンファクトリーおよびSPring-8を利用して解明しました。
ブルーベリーなどで知られるアントシアニンは、植物に広く存在する赤~紫~青色を示す色素成分の一種です。この色素は、アントシアニジンにCτ3GT-Aという酵素が糖を結合することで出来る化合物の総称です。鮮やかな色は食品用色素としてだけでなく、優れた生理活性を示すことから健康食品や医薬品など幅広い分野で利用されています。
アントシアニジンをアントシアニンにするような、糖付加反応を利用すると、水に溶けにくく医薬品として利用できない生理活性物質の可溶性や安定性を高めるなど、有機低分子の化学的および生物学的性質を変えることができます。研究グループでは、チョウマメの花弁に含まれるCτ3GT-Aの立体構造、およびアントシアニジンと結合している状態を解明しました。放射光を用いたX線結晶構造解析を行うには、目的の酵素などを結晶化する必要がありますが、水溶液中で不安定なアントシアニジンと酵素が結合した状態の結晶を得るのは容易ではありません。研究グループは、不安定の要因を、アントシアニジンの酸素原子がプラスの電荷を持つためと考え、アントシアニジンの一種、デルフィニジンとペチュニジンを有機溶媒に溶かしたものを、酵素の結晶を含む水溶液に添加するなど、工夫をして結合状態の結晶を得ることに成功しました。これは、酵素に結合した状態で、プラスの電荷を帯びたアントシアニジンの分子構造を世界で初めて明らかにした例になります。
またフラボノールの一種で、アントシアニジンとは発色の異なるケンフェロールに対する糖転移活性について調べたところ、デルフィニジンに比べて約20倍も低いことが分かりました。そこでケンフェロールとの複合体の立体構造を決定し(図2)、両者の結合した状態を比較してみましたが、その結果は予想とは異なり、デルフィニジンとケンフェロールの結合様式に大きな違いはありませんでした。
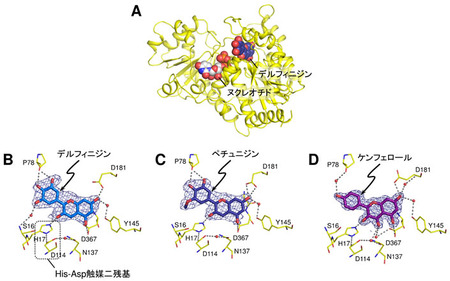
図2 Cτ3GT-Aの立体構造と色素結合部位
(A)タンパク質部分(黄色)に糖ヌクレオチドの一部(炭素原子を白色)とアントシアニジンの一種、デルフィニジン(炭素原子を濃紺)が結合している様子。またデルフィニジン複合体(B)、ペチュニジン複合体(C)、ケンフェロール複合体(D)の各色素原料結合部位の拡大図を示す。色素原料を囲んでいる網(紺色)は、本解析により得られた電子密度を示す。それぞれ異なる糖転移活性を示すにもかかわらず、糖が付加される3位の水酸基は、His-Asp触媒二残基*と同様に相互作用している。
画像提供:日本原子力研究開発機構
一般に、基質と酵素の関係は「鍵」と「鍵穴」の関係に例えられ、酵素(Cτ3GT-A)は結合する分子(アントシアニジンやフラボノール)の構造の違いを見分けていると考えられています。しかし今回の結果は、両者の違いを識別しているのではなく、むしろ両者に共通の構造を認識していることが分かりました。このことから、Cτ3GT-Aの基質認識は酵素としてはむしろ寛容であり、様々な低分子化合物への糖の付加を可能とする人工酵素をデザインする上で、有用な土台になると期待されます。
日本原子力研究開発機構発表のプレスリリースはこちら【JAEA HPへ】